1. 紫外光由此可见稀释谱线造成的基本原理
紫外光由此可见稀释谱线是虽然大分子(或阳离子)稀释紫外光或是由此红外线(通常来说200-800 nm)后再次出现电子零件层的光子所引发的。虽然电子零件间能阶光子的与此同时常常充斥着阻尼和旋转能阶间的光子,因而紫外光由此可见谱线呈现出宽谱带。
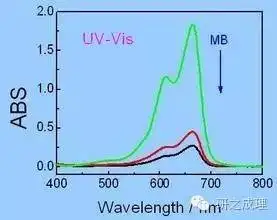
紫外光由此可见稀释谱线的横坐标为红外线(nm),横坐标为无腺度。紫外光由此可见稀释谱线有三个关键的特点:最小稀释峰边线(λmax)和最小稀释峰的安德森无腺常数(κmax)。最小稀释峰所相关联的红外线代表者着氧化物在紫外光由此可见谱线中的特点稀释。而其所相关联的安德森稀释常数是定量的依照。
紫外光由此可见稀释谱线中重要的基本概念:
头分林团:造成紫外光或是由此可见稀释的单糖双键,通常是具备n电子零件和π电子零件的双键,如C=O, C=N等。当再次出现三个头分林团对偶时,三个头分林吕齐县造成的稀释带将消亡,原本的是捷伊对偶稀释带,其红外线比单个头分林团的稀释红外线长,气压也进一步增强。
助色团:这类无紫外光稀释,但能使头分林团稀释峰强化或(和)使稀释峰光行差的双键,如OH,Cl等
光行差:最小稀释峰向长红外线路径终端。
辉光:最小稀释峰向短红外线路径终端。
增(减)色负面效应:使稀释气压进一步增强(弱化)的负面效应。
2. 电子零件层光子的类别和稀释带
A. 碳氢氧化物的电子零件层光子
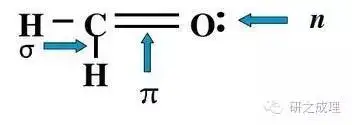
在有机氧化物大分子中有形成单键的σ电子零件、形成单糖键的π电子零件和未成键的孤对n电子零件。当大分子稀释紫外光或是由此可见辐射后,这些外层电子零件就会从基态(成键轨道)向激发态(反键轨道)光子,主要的光子方式有四种,所需能量大小顺序为:σ→σ* >n→σ*>π→π*>n→π*。
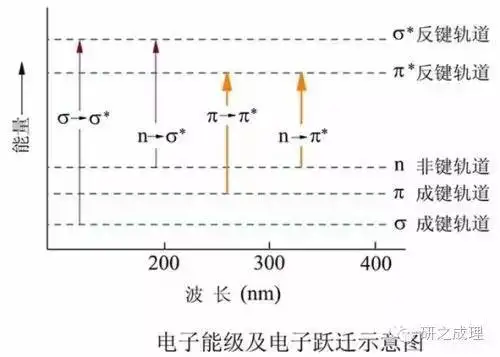
σ→σ*光子:稀释能量较高,通常再次出现在真空紫外光区。饱和烃中的C-C属于这种光子类别。如乙烷C-C键σ→σ*光子,λmax为135nm。(注:虽然通常紫外光由此可见分光亮度计只能提供190~850nm范围的单色光,因而无法检测σ→σ*光子)
n→σ*光子:含有O、N、S等杂原子的双键,如-NH2、-OH-、-SH等可能造成n→σ*光子,安德森无腺常数较小。
π→π*光子:有π电子零件的双键,如C=C,C≡C,C=O等,会再次出现π→π*光子,通常位于近紫外光区,在200 nm左右,εmax≥104 L·mol-1·cm-1,为强稀释带。
K带:对偶体系的π→π*光子又叫K带,与对偶体系的数目、边线和取代基的类别有关。
B带:芳香族氧化物的π→π*光子而造成的精细结构稀释带叫做B带。
E带:E带是苯环上三个双键对偶体系中的π电子零件向π*反键轨道光子的结果,可分为E1和E2带(K带)。苯的B带和E带如下图所示。
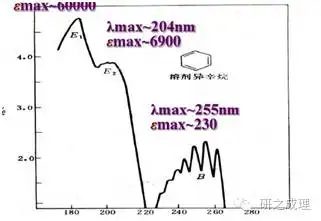
n→π*光子:含有杂原子的单糖双键:如C=O,C=S,-N=N-等双键会再次出现n→π*。再次出现这种光子能量较小,稀释再次出现在近紫外光或是由此红外线区。特点是气压弱,安德森无腺常数小,造成的稀释带也叫R带。
以上各稀释带相对的红外线边线由大到小的次序为:R、B、K、E2、 E1 ,但通常K和E带常合并成一个稀释带。
B.无机物中的电子零件光子
无机氧化物的紫外光由此可见稀释主要是由电荷转移光子和配位场光子造成。
电荷转移光子:无机络合物中心阳离子和配体之间再次出现电荷转移:
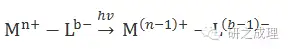
上述公式中心阳离子(M)为电子受体,配体(L)为电子零件给体。不少过渡金属阳离子和含有头分林团的试剂反应生成的络合物和许多水合无机阳离子均可造成电荷转移光子。
电荷转移稀释谱线再次出现的红外线边线,取决于电子零件给体和电子零件受体相应电子零件轨道的能量差。通常,中心阳离子的氧化能力越强,或配体的还原能力越强(相反,若中心阳离子的还原能力越强,或配体的氧化能力越强),则再次出现电荷转移光子时所需能量越小,稀释谱线红外线光行差。
配位场光子:元素周期表中第4和第5周期过渡元素分别含有3d和4d轨道,镧系和锕系元素分别有4f和5f轨道。这些轨道能量通常来说是简并(相等)的,但是在络合物中,虽然配体的影响分裂成了几组能量不等的轨道。若轨道是未充满的,当稀释光后,电子零件会再次出现跃迁,分别称为d-d光子和f-f光子。
3. 影响紫外光由此可见稀释谱线的因素
对偶负面效应:体系形成大π键,使各能阶间的能量差减小,从而电子零件光子的能量也减小,因而对偶负面效应使稀释再次出现光行差。
溶剂负面效应:1.虽然溶剂的存在使溶质溶剂再次出现相互作用,使精细结构消亡。
2. 对π→π*光子来讲,溶剂极性增大时,稀释带再次出现光行差;对于n→π*光子来讲,稀释谱线再次出现辉光。
3. 不同氧化物在不同pH下存在形态不同,稀释峰会随pH再次出现改变。
如苯酚在碱性介质中形成苯酚阴阳离子,其稀释峰从210.5和270nm光行差到235nm和287nm。
4. 紫外光由此可见稀释谱线的应用基本原理
A. 定性基本原理
虽然各种物质具备各自不同的大分子、原子和不同的大分子空间结构,其稀释光能量的情况也就不会相同,因而,每种物质就有其特有的、固定的稀释谱线曲线。碳氢氧化物能采用与标准有机氧化物图谱对照,虽然紫外光谱线反应的是大分子中头分林团和助色团的特性,因而具备相同双键的氧化物稀释谱线类似。因而,也要和其他方法结合才能进行结构分析。

B. 定量基本原理—朗伯比尔定律

注意:运用朗伯比尔定律时,溶液一定要是稀溶液。
5. 紫外光由此可见稀释谱线的特点
1. 灵敏度高:可测10-7-10-4g/mL的微量组分。
2. 准确度高:相对误差在1%-5%之内。
3. 适用范围广:既能进行定量,又可进行定性分析和结构分析(主要分析大分子中官能团)。既可用于无机氧化物的分析,又可进行有机氧化物的分析等。
4. 操作简单,快捷
——————————————————————————————————————————–
再补充一波紫外光漫反射谱线的基本基本原理
1.紫外光由此可见谱线利用的哪个波段的光?
紫外光光的红外线范围为:10-400 nm; 由此红外线的红外线范围:400-760 nm; 红外线大于760 nm为红外光。红外线在10-200 nm范围内的称为远紫外光光,红外线在200-400 nm的为近紫外光光。而对于紫外光由此可见谱线仪而言,人们通常利用近紫外光光和由此红外线,一般测试范围为200-800 nm.
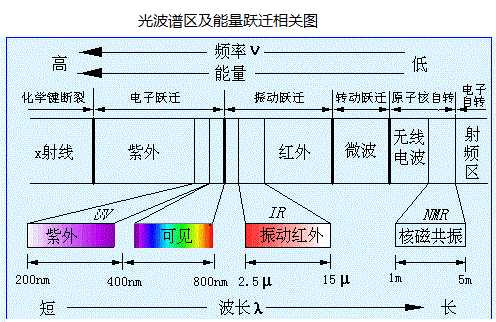
2. 紫外光由此可见漫反射谱线能做什么?
紫外光由此可见漫反射(UV-Vis DRS)可用于研究固体样品的光稀释性能,催化剂表面过渡金属阳离子及其配合物的结构、氧化状态、配位状态、配位对称性等。
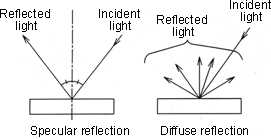
3. 漫反射是什么?
当光束入射至粉末状的晶面层时,一部分光在表层各晶粒面造成镜面反射(specular reflection);另一部分光则折射入表层晶粒的内部,经部分稀释后射至内部晶粒界面,再再次出现反射、折射稀释。如此多次重复,最后由粉末表层朝各个路径反射出来,这种辐射称为漫反射光(diffuse reflection)。
4. 紫外光由此可见谱线的基本基本原理
对于紫外光由此可见谱线而言,不论是紫外光由此可见稀释还是紫外光由此可见漫反射,其造成的根本原因多为电子零件光子.
碳氢氧化物的电子零件光子包括n-π,π-π光子等将放在紫外光由此可见分光分度法中来介绍。
对于无机物而言:
a. 在过渡金属阳离子-配位体体系中,一方是电子零件给予体,另一方为电子零件接受体。在光激发下,再次出现电荷转移,电子零件稀释某能量光子从给予体转移到接受体,在紫外光区造成稀释谱线。其中,电荷从金属(Metal)向配体(Ligand)进行转移,称为MLCT;反之,电荷从配体向金属转移,称为LMCT.
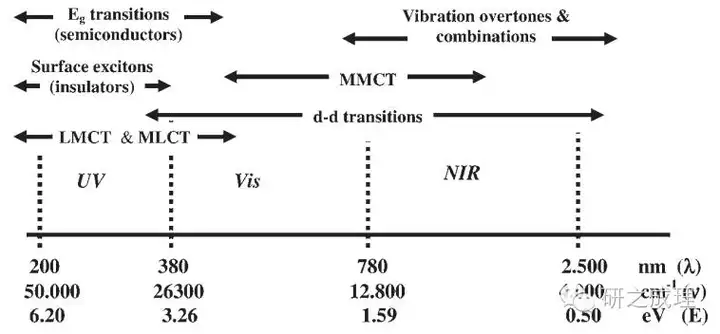
b. 当过渡金属阳离子这类稀释光子激发再次出现内部d轨道内的光子(d-d)光子,引发配位场稀释带,需要能量较低,表现为在由此红外线区或近红外区的稀释谱线。
c. 贵金属的表面等阳离子体共振:
贵金属可看作自由电子零件体系,由导带电子零件决定其光学和电学性质。在金属等阳离子体理论阳离子体振荡频率相与此同时,就会造成共振。这种共振,在宏观上就表现为金属纳米粒子对光的稀释。金属的表面等阳离子体共振是决定金属纳米颗粒光学性质的关键因素。虽然金属粒子内部等阳离子体共振激发或虽然带间稀释,它们在紫外光由此红外线区域具备稀释谱带。
5. 紫外光由此可见漫反射谱线的测试方法——积分球法
积分球又称为光通球,是一个中空的完整球壳, 其典型功能就是收集光。积分球内壁涂白色漫反射层(通常为MgO或是BaSO4),且球内壁各点漫反射均匀。光源S在球壁上任意一点B上造成的光照度是由多次反射光造成的光照度叠加而成的。
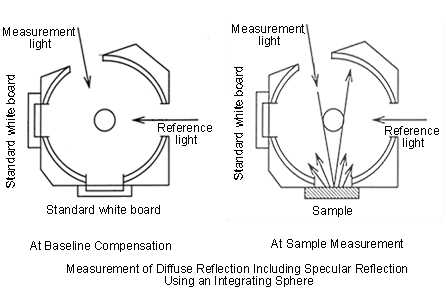
采用积分球的目的是为了收集所有的漫反射光,而通过积分球来测漫反射谱线的基本原理在于:虽然样品对紫外光由此红外线的吸收比参比(通常为BaSO4)要强,因而通过积分球收集到的漫反射光的信号要弱一些,这种信号的差异能转化为紫外光由此可见漫反射谱线。采用积分球能避免光收集过程引发的漫反射的差异。
6. 漫反射定律(K-M方程)
漫反射定律描述一束单色光入射到一种既能稀释光,又能反射光的物体上的光学关系。

注意点:
1. 实际上,从上面的积分球方法中我们也能看出,人们通常来说测量的不是绝对反射率R∞,而是一个相对于标准样品(通常为BaSO4)的相对反射率。
2. 样品的漫反射和入射光红外线相关
3. 在一个稀释的物种的情况下F(R∞)正比于物种的浓度,类似于朗伯比尔定律(将在紫外光由此可见分光亮度法中介绍)








